Die weltweit erste galvanische Zelle wurde von Luigi Galvani entwickelt. Lesen Sie mehr über ihre Geschichte. in diesem ArtikelIm Wesentlichen handelt es sich um eine temporäre Stromquelle, die durch eine chemische Reaktion erzeugt wird. Der Elektronenfluss entsteht durch die Wechselwirkung zweier unterschiedlicher Metalle. Dadurch wird chemische Energie in elektrische Energie umgewandelt, die dann im Alltag genutzt werden kann.
Eine Konzentrationsgalvanische Zelle ist eine Stromquelle, die aus zwei identischen Metallelektroden besteht, die in ein Gemisch aus Salzen dieses Metalls in verschiedenen Konzentrationen getaucht sind.
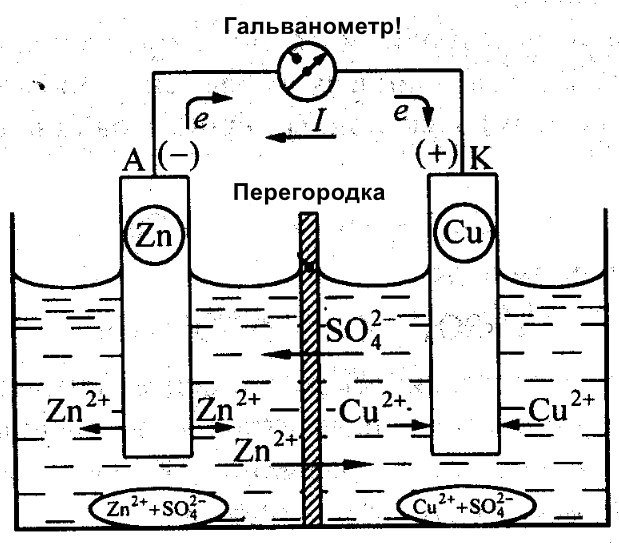
Neben Galvani arbeitete auch Daniel Jacobi an der Entwicklung einer effizienten Batterie. Er modifizierte seine Energiequelle leicht. Sie besteht aus einer in CuSO₄ getauchten Kupferplatte und einer in ZnSO₄ eingetauchten Zinkplatte. Um eine direkte Wechselwirkung zu verhindern, befindet sich zwischen ihnen eine poröse Wand. Unten ist ein Diagramm von Daniel Jacobis galvanischer Zelle abgebildet.
Zink und Kupfer weisen unterschiedliche Reaktivität auf, wodurch sich ihre Ladung unterscheidet. Folglich sind auch die Ladungsniveaus der Elektroden nicht einheitlich. Dies ermöglicht ihre Bewegung und erzeugt einen elektrischen Strom. Dieser Strom fließt, sobald eine Person oder der Erfinder eines Stromspeichers einen Verbraucher anschließt. Dieser Verbraucher kann beispielsweise eine Glühbirne, ein Radio, eine Computermaus oder ein anderes elektrisches Gerät sein.
- Schematische Darstellung einer galvanischen Zelle
- Der Aufbau einer galvanischen Zelle
- Das Funktionsprinzip einer galvanischen Zelle
- Antworten auf häufig gestellte Fragen
- Arten von galvanischen Zellen
- Tabelle der galvanischen Zellen
- Zweck einer galvanischen Zelle
- Galvanische Zelle zu Hause
- Herstellungsprozess
Schematische Darstellung einer galvanischen Zelle
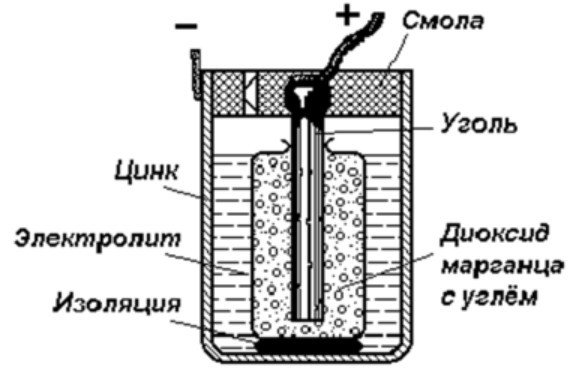
Ein Schaltplan beschreibt die Zusammensetzung und den Aufbau einer galvanischen Zelle. Sie kann aus verschiedenen chemischen Elementen mithilfe von Hilfsvorrichtungen aufgebaut werden. Im Folgenden wird der Aufbau einer galvanischen Zelle kurz erläutert. Lesen Sie mehr darüber in diesem Artikel.!
Der Aufbau einer galvanischen Zelle
Das einfachste Energiespeichergerät besteht aus:
- Kohlestange.
- Zwei unterschiedliche Metalle.
- Elektrolyt.
- Harz oder Kunststoff.
- Isolator.
Wie aus diesem Diagramm ersichtlich, besteht eine galvanische Zelle aus einer negativen und einer positiven Elektrode. Sie können aus Kupfer, Zink oder anderen Metallen gefertigt sein. Man nennt sie Kupfer-Zink-Zellen. TrockenbatterienDie
Bezeichnung einer galvanischen Zelle in einem Diagramm Es besteht aus zwei nahe beieinander liegenden, vertikalen Linien. Eine der Linien ist kürzer. An den Enden jeder Linie befinden sich Symbole. PolaritätDie lange Linie ist als Pluspol, die kurze als Minuspol gekennzeichnet. Die Spannung kann daneben angegeben sein. Das bedeutet, dass der Stromkreis, der mit der Batterie betrieben wird, nur bei dieser Spannung funktioniert.
Das Funktionsprinzip einer galvanischen Zelle
Eine galvanische Zelle funktioniert durch die Bewegung von Elektronen zwischen zwei Metallkontakten. Dabei findet eine chemische Reaktion statt. Lesen Sie mehr über die Thermodynamik einer galvanischen Zelle und die Entstehung galvanischer Elektrizität. HierDie
Antworten auf häufig gestellte Fragen
| Galvanisch | Erläuterung |
| Batterie | Eine Energiequelle, die durch Prozesse in einem begrenzten, miniaturisierten Raum funktioniert. Konkret wird Energie durch eine chemische Reaktion erzeugt. |
| Voltaische Zelle oder Voltaische Säule | Dies ist ein Energieelement, das erstmals von einem Wissenschaftler namens Volt entwickelt wurde. |
| Verfahren | Die Wechselwirkung zwischen chemischen Elementen, die zur Bildung eines elektrischen Stroms führt. |
| Entladung | Dies ist der Abschluss einer chemischen Reaktion. Das heißt, es findet keine Wechselwirkung zwischen den Substanzen statt. Galvanische Entladung ist in Warframe vorhanden. Im Wesentlichen handelt es sich um eine seltene Modifikation. Sie wird für Nahkampfwaffen verwendet. PolaritätV2. |
| Galvanischer Kontakt | Dies ist der Kontakt zwischen den Elektroden und der Lösung. |
| Wirkung | Das Auftreten eines Unterschieds zwischen zwei Kontakten aus zwei verschiedenen Metallen. Die Stärke dieses Unterschieds hängt von der Temperatur und der chemischen Zusammensetzung der Leiter ab. Im Wesentlichen handelt es sich dabei um Voltas erstes Gesetz. |
| Verbindung/Glied/Kette | Zwei oder mehr Abschnitte eines Stromkreises an eine Stromquelle anschließen. |
| Galvanische Ladung | Die Batterie wird mit Energie aufgeladen. |
Die Galvanisierung ist ein chemisches Verfahren, bei dem elektrischer Strom eingesetzt wird. Die Reaktion reduziert die Menge der gelösten Metallkationen so weit, dass diese schließlich eine gleichmäßige Beschichtung auf einer Metallelektrode bilden. Dadurch wird das Werkstück haltbarer, kleine Dellen verschwinden und sein Aussehen verbessert sich.
Arten von galvanischen Zellen
Es gibt eine Reihe spezifischer Batterietypen.
Tabelle der galvanischen Zellen
| Typ | Stromspannung | Hauptvorteile |
| Lithium | 3 V | Groß Kapazität, hoher Strom. |
| Salzbatterien oder Kohlenstoff-Zink | 1,5 Zoll | Am günstigsten. |
| Nickeloxyhydroxyl NiOOH | 1,6 Volt | Hohe Stromstärke. Hohe Kapazität. |
| Alkalisch oder alkalisch | 1,6 V | Hohe Stromstärke. Gute Lautstärke. |
Dieses Thema wird im Artikel ausführlicher behandelt. Batterietypen!
Zweck einer galvanischen Zelle
Es dient zum Starten elektrischer Geräte. Dazu gehören beispielsweise:
- Betrachten.
- Fernbedienungen.
- Taschenlampen.
- Medizinische Geräte.
- Laptops.
- Spielzeug.
- Schlüsselanhänger.
- Telefone.
- Laserpointer.
- Taschenrechner.
Und ähnliche Dinge um uns herum.
Galvanische Zelle zu Hause
Sie können selbst eine einfache Stromquelle herstellen. Dazu benötigen Sie folgende Materialien:
- Plastikbecher.
- Elektrolyt. Dies kann eine Kochsalzlösung, Soda oder in Wasser verdünnte Zitronensäure sein.
- Platten aus zwei verschiedenen Metallen. Zum Beispiel Aluminium und Kupfer.
- Drähte
Herstellungsprozess
Nehmen Sie einen Plastikbecher und füllen Sie ihn mit dem Elektrolyten. Füllen Sie ihn nicht bis zum Rand; es ist besser, 1–2 Zentimeter unter dem Rand zu lassen. Verbinden Sie die Drähte mit den Metallplatten. Platzieren Sie anschließend die Kupfer- und Aluminiumplatten an den Rändern des Behälters. Sie sollten parallel zueinander ausgerichtet sein. Sobald alles vorbereitet ist, können Sie die Spannung mit einem Voltmeter messen.
Schließen Sie das Gerät an und berühren Sie mit den Messspitzen die Kontakte unserer Stromquelle. Halten Sie sie so lange gedrückt, bis die Anzeige eine Spannung anzeigt. Diese beträgt üblicherweise 0,5–0,7 Volt. Die Werte können je nach Elektrolyt bzw. genauer gesagt, der als Elektrolyt verwendeten Substanz variieren.
So wird eine selbstgebaute galvanische Zelle hergestellt.