Die weitverbreitete Nutzung kleiner Haushaltsgeräte durch Verbraucher erfordert Stromquellen bzw. Einzelstromkreise. galvanische ZellenBatterien, allgemein bekannt als elektrische Batterien, wurden erstmals im Jahr 1800 von dem italienischen Physiker Alessandro Volta erfunden. Sie unterscheiden sich in Größe, Form, Spannung, Kapazität und Batterietyp. Alkali- und Salzsäurebatterien finden breite Anwendung in Haushaltsgeräten und Elektronikgeräten.
Was sind Salzbatterien?
Salzbatterien Kohle-Zink-Batterien sind einfache elektrische Stromquellen, die durch eine chemische Reaktion in einem Gerät erzeugt werden. Sie werden auch als Kohle-Zink-Batterien oder Kohle-Batterien bezeichnet. Dieser Zelltyp gilt als der günstigste, hat aber eine geringe Energiedichte und eignet sich daher gut für Geräte mit geringem Stromverbrauch. In Geräten mit hohem Stromverbrauch oder charakteristischen Laststrom- und Temperaturspitzen halten sie nicht lange und werden daher nicht eingesetzt.
Bezeichnung von Salzbatterien
Die Bezeichnung von Salzbatterien erfolgt nach verschiedenen Normen:
- Amerikanisches Klassifizierungssystem.
- Internationales System (IEC).
- Zwischenstaatlicher Standard (GOST).
| Amerikanisches Klassifizierungssystem | Internationale Klassifikation IEC | GOST | Größe, mm | Kapazität, mAh |
| A | R23 | 17x50 | ||
| AA | R6 | 316 | 14,5 x 50,5 | 1100 |
| AAA | R03 | 286 | 10,5 x 44,5 | 540 |
| C | R14 | 343 | 26,2x50 | 3800 |
| D | R20 | 373 | 34,2 x 61,5 | 8000 |
| F | R25 | 33x91 | ||
| 1/2AA | R14250 | 312 | 14,5 x 25 | 250 |
| R10 | R10 | 332 | 21,5 x 37,3 | 1800 |
Die Kennzeichnung einer Salzbatterie mit R 6 bedeutet beispielsweise: rund, zylindrisch, FingerSalzelement, Gesamtabmessungen 14,5 x 50,5 Kapazität1100 mAh. Die Standardspannung beträgt 1,5 V. Die Kennzeichnung „R“ (Salz) auf dem Batterieetikett unterscheidet Salzbatterien von anderen Batterietypen (Alkaline- oder Lithiumbatterien).
Gestaltung und Komposition
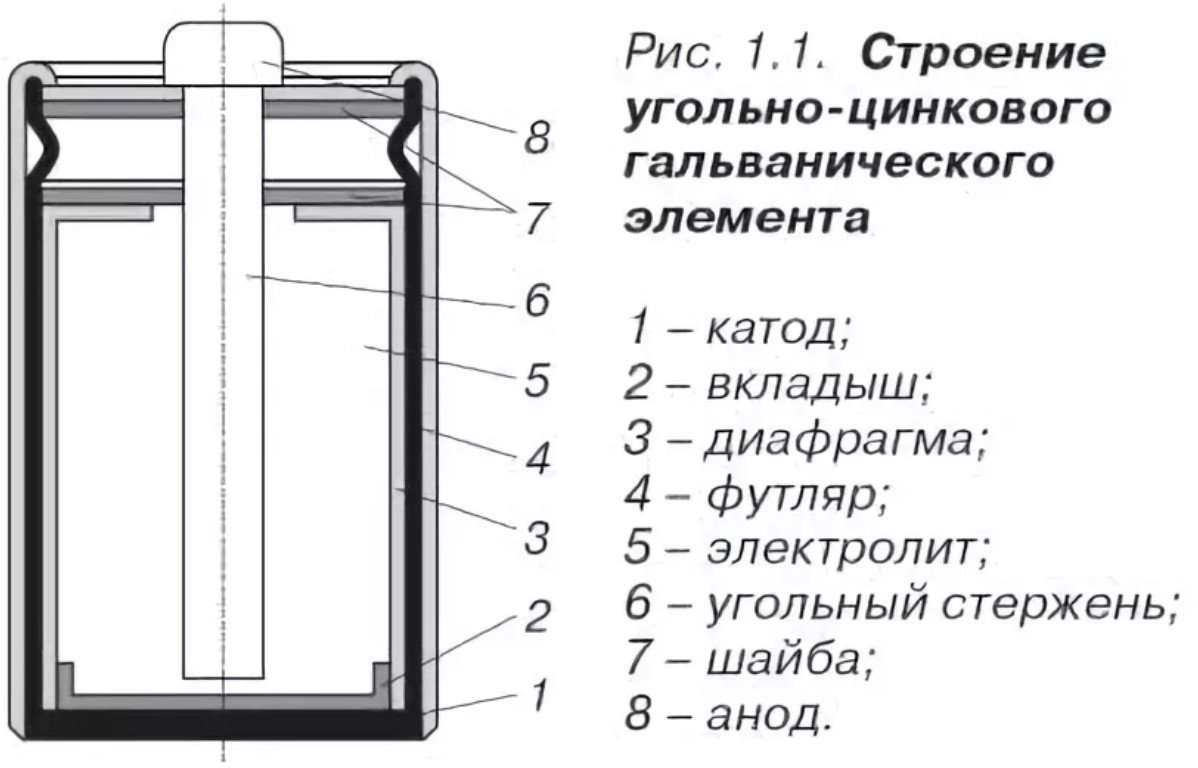
Der Aufbau einer Salzbatterie ist recht einfach und besteht aus:
- Kathode - die gleiche Das Gehäuse der Salzbatterie ist hergestellt aus Zink, mit verbesserten Korrosionsschutzeigenschaften und einem hohen Reinheitsgrad (minus).
- Die Anode ist ein durch Pressen hergestelltes Agglomerat, das mit Elektrolyt imprägniert ist (plus).
- Elektrolyt: Ammoniumchlorid oder Zinkchlorid, mit Zusatz eines Verdickungsmittels (Stärke).
- Kohlenstoffstromleiter - verläuft durch die Mitte, behandelt mit einer Paraffinmischung.
- Gaskammer - befindet sich oben und dient zum Auffangen von Gasen aus der chemischen Reaktion.
- Dichtung – befindet sich oben und dient als Dichtmittel.
- Schutzhülle – aus Pappe oder Blech zum Schutz vor Korrosion und Elektrolytaustritt.
Betrachten wir die Zusammensetzung einer Salzbatterie aus chemischer Sicht:
- Die Kathode besteht aus hochreinem Zink und ist korrosionsbeständig.
- Anode - MnO-Mischung2, Graphit, Elektrolytimprägnierung.
- Als Elektrolyt dient Ammoniumchlorid oder eine Mischung aus Zinkchlorid und Calciumchlorid.
Welche Batterien sind besser: Salzbatterien (1) oder Alkalibatterien (2)?
Der Vergleich kann in Form einer Tabelle erfolgen, in der die Vor- und Nachteile verschiedener Elementtypen deutlich erkennbar sind:
| Vergleichsparameter | 1 | 2 |
| Temperaturbedingungen, Betriebsbedingungen | Die Leistungsfähigkeit ist bei niedrigen Temperaturen reduziert und das Gerät ist nicht beständig gegen Stromspitzen. | Funktioniert gut bei niedrigen Temperaturen – bis zu -20 °COSie widerstehen Spannungsspitzen problemlos und schrecken vor einem plötzlichen Anstieg des Laststroms nicht zurück. |
| Haltbar bis | 2-3 Jahre | 5 Jahre |
| Anwendung | Geeignet für den Einsatz in Geräten mit geringem Stromverbrauch | Geeignet für den Einsatz in Geräten mit mittlerem und hohem Energieverbrauch |
| Instrumente, technische Geräte | Wecker, Wanduhren, Fernbedienungen, Mini-Taschenlampen, einfaches Spielzeug | Abspielgeräte, Taschenlampen, Musikspielzeug, Diktiergeräte, Blutdruckmessgeräte |
Bei der Auswahl einer Stromquelle für ein Gerät mit speziellen Betriebsanforderungen ist es wichtig, den Unterschied zwischen einer Salzsäurebatterie und einer Alkalibatterie zu kennen. Salzsäurebatterien sind mit dem Buchstaben R gekennzeichnet, Alkalibatterien hingegen mit dem Buchstaben L (LR).
Schlussfolgerungen und Empfehlungen
Diese Art von Stromquelle ist leichter und kostengünstiger. Allerdings ist die Lagerfähigkeit von Salzsäurebatterien mit zwei bis drei Jahren begrenzt, und sie können sich während der Lagerung sowie im Betrieb, insbesondere bei plötzlichen Stromspitzen, teilweise selbstentladen. Angesichts ihrer vergleichsweise geringen Leistung, aber des niedrigen Preises, ist es daher ratsam, mehrere Batteriesätze als Reserve anzuschaffen.
Nicht groß KapazitätSalzbatterien (2-3 Mal geringer als andere Batterietypen) sind daher nur für einfache Geräte mit niedrigem Laststrom geeignet.
Ob man Salzbatterien aufladen kann, lässt sich leicht feststellen: Die Bezeichnung der Batterie ist auf dem Gehäuse des zum Aufladen vorgesehenen Geräts angegeben. KapazitätDie Kapazität wird in mAh angegeben. Ist dieser Wert nicht verfügbar, handelt es sich um eine herkömmliche Batterie. Trotz zahlreicher Expertenempfehlungen sollte diese nicht geladen werden. Das Laden bringt nicht die erwartete Langzeitwirkung und kann durch Überhitzung und Elektrolytaustritt zu einem Unfall führen. Benötigen Sie eine zuverlässigere und langlebigere Energiequelle, investieren Sie besser in eine Alkali-Batterie oder einen Akku.
Interessante Tatsache: Selbstgebaute Salzbatterie Es lässt sich ganz einfach herstellen. Sie benötigen 50-Kopeken-Münzen, Alufolie, Papier und eine Salzlösung. Am besten weichen Sie die Münzen vor Gebrauch in Essig ein, um Ablagerungen oder Schmutz zu entfernen. Bauen Sie die Vorrichtung zusammen: eine Münze, in Salzlösung getränktes Papier und Alufolie. Wiederholen Sie diesen Vorgang mehrmals, sodass eine Säule entsteht, mit der Münze (Pluspol) an einem Ende und der Alufolie (Minuspol) am anderen. Der Strom wird durch die Potenzialdifferenz erzeugt, die der Elektrolyt (die Salzlösung) zwischen dem Metall der Folie und der Münze hervorruft. Diese Vorrichtung nennt man Voltasche Säule, und ihre Spannung hängt direkt von der Anzahl der verwendeten Münzen ab: Je mehr Münzen, desto höher die Spannung. Nach dem Experiment sind die Münzen jedoch nicht mehr verwendbar; sie sind rostig.