Eine Batterie funktioniert nach dem Prinzip einer einfachen chemischen Reaktion, die typischerweise zwischen drei Elementen stattfindet. Die dabei entstehende Reaktion erzeugt einen elektrischen Strom. Das ist im Wesentlichen das Prinzip.
Drei Schlüsselobjekte:
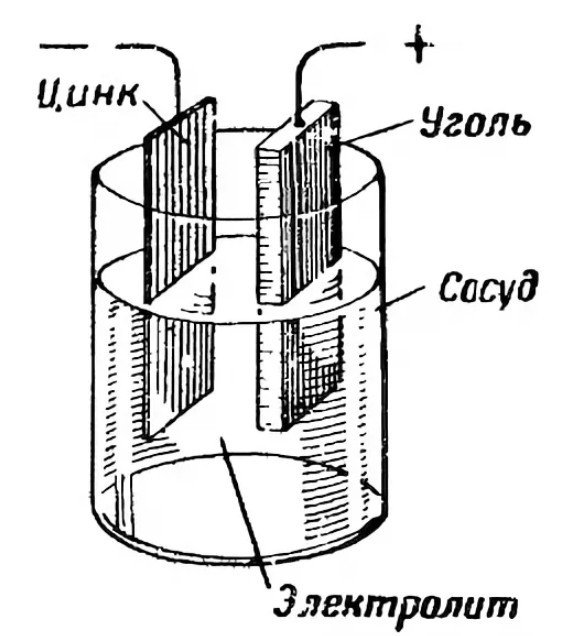
- Anode "+"
- Kathode "-"
- Elektrolyt
Die Anode, der positive Pol, dient als Elektronenquelle. Sie besteht üblicherweise aus Zink. Die beiden Elektroden interagieren über einen Elektrolyten. Dieser Elektrolyt ist typischerweise ein Salz, Ammoniumchlorid oder eine Lauge. Er kann trocken oder flüssig sein. Zur Verdickung fügen Hersteller Polymerverbindungen hinzu. Manche verwenden auch Stärke.
Wie eine Batterie funktioniert
Der Strom fließt vom Pluspol zum Minuspol. Dies geschieht, wenn ein Verbraucher an die Batterie angeschlossen wird. Schon das einfache Verbinden der Plus- und Minuspole mit einem Draht verursacht einen Kurzschluss. Dadurch kann die Batterie schnell entladen und sogar ein Brand entstehen.
Die Kathode fungiert als Reduktionsmittel und nimmt Elektronen von der Anode auf. Im Elektrolyten bewegen sich die Ionen frei und ermöglichen so eine effiziente Stromerzeugung.
Welche chemischen Vorgänge finden statt?
Zum Beispiel in Glas KapazitätGießen wir eine Schwefelsäurelösung hinein und legen einen Zinkstab hinein. Auf der Oberfläche des Stabs befinden sich positiv geladene Ionen. Negative Ionen der Säure sammeln sich um den Zinkgegenstand in der Lösung. Die Lösung übt Anziehungskräfte aus, die die Zinkionen leicht ablösen. Dadurch erhält die Flüssigkeit eine positive Ladung und die Zinkplatte bzw. der Zinkstab eine negative. Physikalisch gesehen entspricht die Potenzialdifferenz der Spannung. Dadurch entsteht ein elektrischer Strom.
Wenn die Säurelösung mit dem Metall in Kontakt kommt, entsteht an der Grenzfläche ein elektrisches Feld. Dabei wird chemische Energie in elektrische Energie umgewandelt. So funktioniert eine Batterie.
Nach einer gewissen Zeit lässt die Kapazität der Batterie nach. Das hängt ganz davon ab, wo und wie die Stromquelle genutzt wird. Beispielsweise halten zwei 1,5-Volt-Batterien bei mäßiger Nutzung einer Taschenlampe etwa einen Monat. Setzt man dieselben Batterien jedoch in ein Elektroauto ein, fährt dieses nur noch wenige Stunden.
Aus all dem können wir schließen, dass sich die Batterie umso schneller entlädt, je größer die Belastung ist.
Lesen Sie auch: